- · 《中国药理学与毒理学杂[09/30]
- · 《中国药理学与毒理学杂[09/30]
- · 《中国药理学与毒理学杂[09/30]
- · 《中国药理学与毒理学杂[09/30]
- · 《中国药理学与毒理学杂[09/30]
乙肝在研新药临床前,应完成毒理学评估,确定
作者:网站采编关键词:
摘要:接上一篇新药开发前,临床前研究的急毒试验很有必要,可以为进入人体第一期临床试验所需要的剂量提供重要参考,包括长毒设计、可能发生突变以及生殖毒性等,提供一个对受试者
接上一篇新药开发前,临床前研究的急毒试验很有必要,可以为进入人体第一期临床试验所需要的剂量提供重要参考,包括长毒设计、可能发生突变以及生殖毒性等,提供一个对受试者最为安全可靠的药物剂量,以及过量的急性中毒数据。
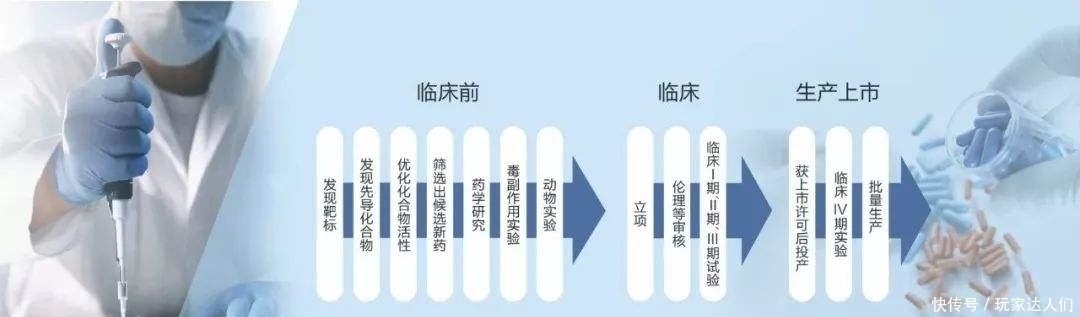
乙肝在研新药临床前,应完成毒理学评估,确定受试者的安全范围
一种新药临床前需要做许多工作,了解正在开发的新药主要毒性靶向器官,是临床前研究制定解毒器官挽救手段的重要一步骤。简单来讲,一种乙肝在研新药的毒性机制必须在临床前就深入了解,对毒向哪些器官,可以制定救治措施。乙肝病毒生命周期有很多步骤,靶向不同步骤用药是当前全球研发的主要理论基础,在仅知道可能对乙肝治疗有效,但无法判断毒性和靶向毒器官时,就需要做单次急毒试验。
都知道,曾经许多药物研发到上市不久即出现耐药性,这个问题在当时是相当棘手,现有的前沿临床前研究通过模拟人体在动物中做试验,发现了新的乙肝病毒标志物,例如,HBV-RNA、cccDNA以及HBV pgRNA,它们能够满足目前提倡的判断功能性治愈标准。包括在猪、猴、小鼠、土拨鼠、鸭、树鼩等动物模型进行模拟人体来用药。

急毒试验过程中,必须完成多项和LD50关联的试验,LD50也在急毒试验中广泛应用。虽然,由于个体差异、给药途径、药性等不同,每个受试的动物最小的导致死亡剂量也会存在巨大差异,但是,在急毒试验中,必须要确定下最小致死量,也就是能够引发动物死亡的在研新药最小剂量单位。查找和受试药物化学相近结构的化合物毒理学详细资料,来设定预试验的剂量范围。
通常给每一组若干动物按照一定剂量递增或者递减来给予用药,给药后,医药技术研发人员记录下动物的死亡数量。找到零死亡组和全死亡组,再按照一定剂量重新试验,目的是测定可以引发动物致死的最大限度剂量和最小剂量,而这就是试验中的上限剂量和下限剂量。在确定上限和下限剂量后,就可以进入真正的动物试验,包括单次或多次动物最大耐受、最大给药、近似致死量以及固定剂量试验。

最后就是得到一份关于急毒试验的报告,当中必须保护给药和观察的方法,试验动物具体名称种类和试验的环境,还有就是报告应该有摘要和供试品等都应该详细记录。急毒报告应该把所开发的新药对某种动物的毒副反应的发生时间、严重程度、持续时间、病理学、死亡时间等记录清楚,病理要有病理组织学报告拍照的照片,最后就是要有病理检查人的名字和药品注册申请人签章。

小番健康结语:人们对于临床试验了解的相当丰富,但对于一种新药进入人体临床前需要进行哪些环节,未必会有所了解。无论是中国还是美国,新药研发前期都必须完成毒理学评估,主要有急毒试验,然后就是长毒,目的是最终确定进入人体临床试验中,给予受试者的用药安全范围、发生毒性反应后的严重程度、毒反应的可逆等,并对毒性靶向的人体器官已有了解。
慢性乙肝治疗的临床治愈,其实并不遥远,伴随全球各大药企和科研单位对乙肝病毒作用机制深刻认识,有些主要靶向病毒不同生命周期,而有些则直接靶向宿主,按照现有医疗水平和研发能力,靶向病毒不同生命周期各个步骤距离临床治愈距离甚远,而靶向乙肝病毒整个复制生命周期的方向,可以实现功能性治愈,包括以下基于乙肝病毒进入肝细胞、cccDNA形成、表面抗原形成分泌、pgRNA以及HBx蛋白等,目前全球多数药企均围绕这些靶点进行开发。
文章来源:《中国药理学与毒理学杂志》 网址: http://www.zgylxydlxzz.cn/zonghexinwen/2021/0220/516.html
上一篇:气体类推进剂申报化妆品新原料时,毒理学试验
下一篇:保健食品及其原料毒理学评价程序